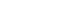腎がんに対する2つの先進的な低侵襲手術による腎部分切除
○世界の標準的手術であるロボット支援腎部分切除
○腎血流非遮断・腎実質無縫合で行うミニマム創内視鏡下腎部分切除
はじめに:小さな腎腫瘍の増加
近年、超音波検査やCT検査などの画像診断の普及に伴い、健康診断や他の病気の検査中に、小さな腎腫瘍が偶然見つかるケースが増加しています1。これらの腎腫瘍は、悪性(腎がん)と良性腫瘍の両者があり、多くの場合は画像診断で良悪性の区別がつきます1。画像診断で悪性(腎がん)と診断された場合、手術が標準的治療になります。ただし小さな腫瘍では、悪性と良性の区別がつきにくい場合もあり、当教室では、より正確な診断のために鑑別診断モデルを開発し2、治療方針の決定に活用しています。悪性が否定できなければ通常は腎がんに準じて治療を行いますが、患者さんの希望により腎腫瘤生検を行い診断を確定することもあります。
腎機能障害(慢性腎臓病:CKD)の患者さんの増加:腎機能温存の意義
最近、慢性腎臓病(Chronic Kidney Disease:CKD)という概念が注目されています。CKDとは、腎障害を示す所見や腎機能低下が慢性的に続く状態で、放置した場合、腎不全となって人工透析や腎移植が必要になることもあります。現在、日本には多数のCKD患者さんがいると言われています。さらに、CKDでは、人工透析に至らなくても、心臓病や脳卒中などの心血管疾患にもなりやすいことが明らかになり、自覚症状のないうちに診断し適切な治療を行うことが大切です。腎がん治療の中心は手術であり、腎臓の片方あるいは一部を摘出するため、術後にある程度は腎機能が低下するリスクがあります。
したがってCKDの患者さんが腎腫瘍と診断された場合、治療に際して特に腎機能温存に留意する必要があります。
腎腫瘍に対する腎部分切除の意義
臨床的に腎がん(疑い含む)と診断された場合、従来は腎臓を周囲の脂肪組織ごと丸ごと全摘出する根治的腎摘除が標準的治療でした。しかしながら、近年、(4cm以下の)小さな腎腫瘍に対し、腫瘍の部分のみを摘出する腎部分切除は、根治性において根治的腎摘除と同等なことが示され、小径腎腫瘍に対する標準治療となっています。根治的腎摘除と比較して、腎部分切除は、健常腎実質が温存されるため、術後の腎機能を保つ上では根治的腎摘除より優れています3。私たちは、根治的腎摘除では術後CKDを高率に発症すること3、その場合心血管疾患にもなりやすいことを報告してきました4。
また画像検査で腎がん(疑い含む)と診断され腎部分切除を行った場合、病理検査で実際は良性腫瘍と診断されることがあります。欧米の複数の施設からの報告では、腎部分切除症例での良性腫瘍の頻度は20-25%と比較的高いと報告されています。 一方、東京科学大学とがん研有明病院の二施設の成績では、腎部分切除を行った患者さんでは良性腫瘍の頻度は11%と欧米よりも低い結果でした5。これは日本では精度の高い画像診断が行えること、またオンコサイトーマという良性腫瘍が日本人(アジア人)では欧米人よりも少ないためではないかと考えられます。腎部分切除の対象となるような比較的小さな腎腫瘍では、良性腫瘍は日本人では欧米人より少ないものの無視できない頻度であることがわかりました。 これらのことから、腎腫瘍に対しては、可能であれば腎部分切除を行うことがよいと考えられます。ただし、全ての腎腫瘍に腎部分切除が行えるものではなく、腫瘍の大きさと位置が重要な条件となります。径4cm以下の腫瘍は、ほとんどの腫瘍が腎部分切除の対象となります。4cm以上の腫瘍においても、腫瘍の位置と大きさによっては腎部分切除を行うことも可能です。
従来は、腎部分切除の多くは開腹手術で行われてきました。最近では、腹腔鏡手術やロボット支援手術など新たな低侵襲手術(患者さんの体の負担が少ない手術)による腎部分切除を行う施設が増えており、なかでもロボット支援腎部分切除は世界の標準的手術となっています。当教室では、腎がんに対するロボット支援腎部分切除およびミニマム創内視鏡下無阻血・無縫合腎部分切除を行っています。
世界の標準的手術であるロボット支援腎部分切除
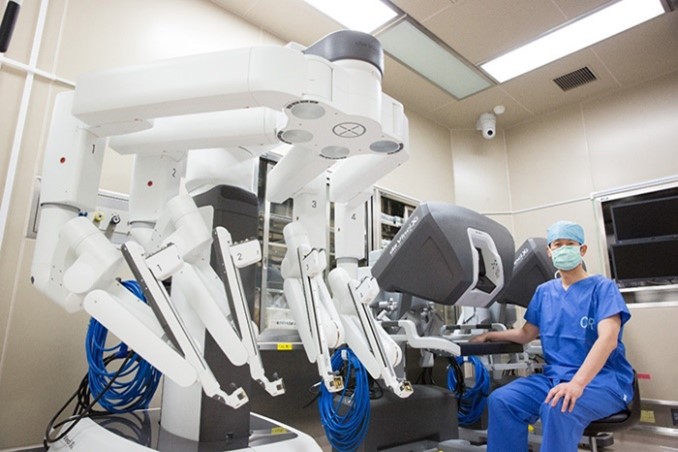
東京科学大学では、2017年9月に手術支援ロボット「ダビンチ(da Vinci)Xi」による手術を開始、2020年7月には2台目の手術支援ロボットda Vinci Xを導入しました。ロボット支援手術は、手術支援ロボットを用いて行う腹腔鏡手術であり、従来の腹腔鏡手術の利点をさらに向上させることができると考えられています。ロボット支援手術では、術者はコンソールという機器から、鮮明なハイビジョン3D画像を見ながら、コントロールハンドルで精密な手術操作を行います。
ロボット支援手術は、その特長として、ロボットの鉗子先端の可動域が広く、手ぶれ防止機能があり、気腹(お腹を炭酸ガスで膨らませる)による出血の低減、3D内視鏡画像による良好な視野のもと手術を行うことができます。このため、ロボット支援手術では、従来の腹腔鏡手術や開腹手術よりも、繊細かつ丁寧な、そして確実な手術操作が可能となります。具体的には、ロボット支援腎部分切除は開腹手術と比較して、皮膚切開が小さく術後の痛みが少ないことに加え、合併症や出血が少なく、入院期間が短いと報告されています。また、通常、腎部分切除では腎腫瘍切除の際の出血を減らすために、一時的に腎臓への血流を遮断する必要がありますが、ロボット支援手術ではその血流遮断時間が腹腔鏡手術よりも短時間で済み、術後の腎機能低下もより小さいとされています。そのほか、ロボット支援手術では、腹腔鏡手術と比べ、開腹手術や腎摘除術への移行率が低く、入院期間が短いと報告されています。このような、優れた利点や低侵襲性を有することから、現在、欧米や本邦においてロボット支援腎部分切除は腎がんに対する標準的手術となっています。
ロボット支援腎部分切除の手術適応は7cm以下の腎がんです。腫瘍の位置と大きさによっては、本手術の適応とならないこともありますので、本手術をご希望の方は外来担当医へお問い合わせください。
腎血流非遮断・腎実質無縫合で行うミニマム創内視鏡下腎部分切除
当教室では、患者さんの体の負担(侵襲)を最小限にする腎部分切除の術式の開発を行ってきました6。当教室で開発、実践しているミニマム創内視鏡下腎部分切除では、皮膚切開がミニマムなだけではなく、最大限の腎機能温存を企図して、腎血流の非遮断・腎実質の無縫合を原則としています。特に腎臓が片方しかない患者さんや、腎機能が悪い患者さんに適した体に優しい手術と言えます。
腫瘍が4cm未満であれば、腫瘍の位置に関わらず、ほとんどがミニマム創内視鏡下腎部分切除の手術適応になります。また4cm以上の腫瘍でも、腫瘍の位置によっては本手術の適応になります。
ミニマム創内視鏡下腎部分切除は、5cm程度の皮膚切開で手術を行い、術後の疼痛や皮膚のしびれが小さい手術です6-9。体内に炭酸ガスを注入せず、腎血流を遮断せずに行います。必要に応じ、腎血流を遮断することもありますが、現在ではほぼ全例で、腎血流の遮断を行っていません。また、原則として、腫瘍を切除した後の止血を目的とした腎実質の縫合も行っていません。この結果、術後の腎機能が良好に保たれ10、腎部分切除の合併症の一つである術後仮性動脈瘤の発生を殆ど認めていません11。
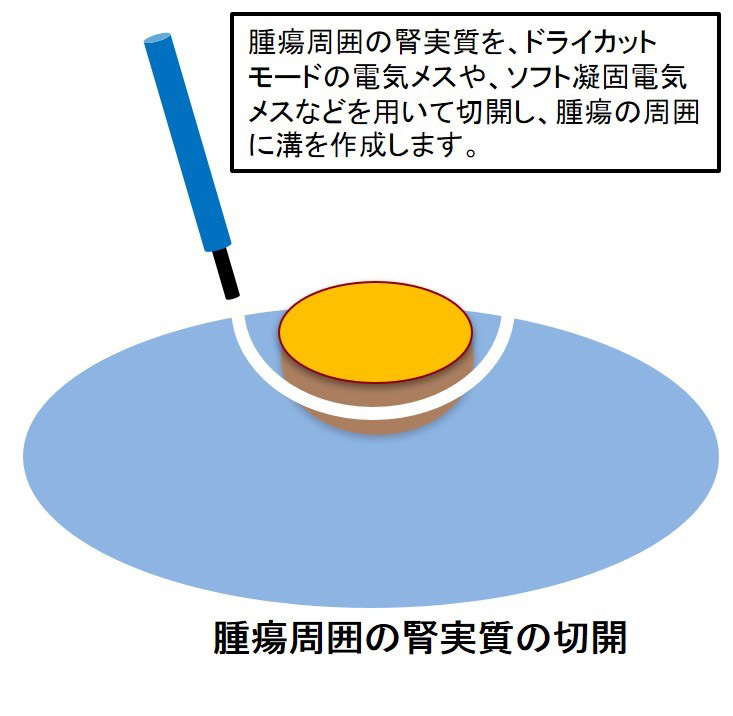
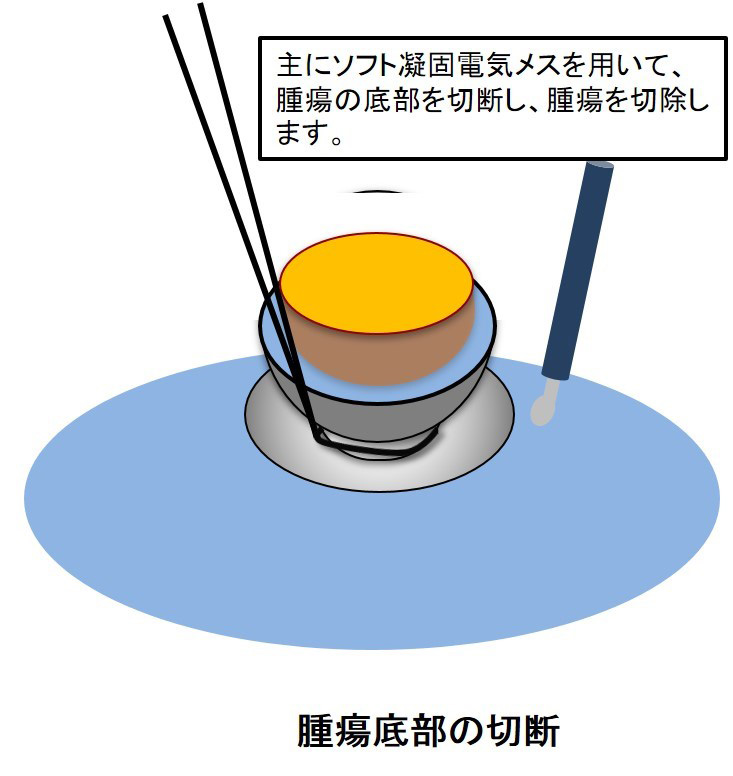
実際の手順ですが、まず腫瘍周囲の正常腎実質に電気メスなどを用いて、腫瘍の概形を形作るよう腫瘍周囲に溝を形成します。さらに腫瘍の底部の切開を進めて、腫瘍を切除します。この際にソフト凝固デバイスなどを用いて、丹念に止血を行いながら腫瘍部分を摘出します。本術式は、手技的にも特別に困難なものではなく、安定した成績が得られています12。 現在、ミニマム創内視鏡下腎部分切除は、3D 内視鏡+ヘッドマウントモニターシステムを使用し、明瞭な立体拡大視野で精緻な手術操作を行っています13。