Matsuoka Y, Tanaka H, Kimura T, Waseda Y, Uehara S, Yasuda Y, Kijima T, Yoshida S, Yokoyama M, Ishioka J, Saito K, Kihara K, Fujii Y. The role of MRI-targeted biopsy in prediction of adverse pathological and oncological outcome after radical prostatectomy. The 114th annual meeting of the American Urological Association. San Francisco, USA, 2018/5/20
Matsuoka Y, Tanaka H, Kimura T, Waseda Y, Uehara S, Yasuda Y, Kijima T, Yoshida S, Yokoyama M, Ishioka J, Saito K, Kihara K, Fujii Y. Characteristics of global Gleason grading for MRI-targeted biopsy in comparison with systematic biopsy and prostatectomy grades. The 33rd Annual Congress of the European Association of Urology. Copenhagen, Denmark, 2018/3/19
Matsuoka Y, Uehara S, Yoshida S, Tanabe K, Tanaka H, Kimura T, Moriyama S, Yasuda Y, Kijima T, Yokoyama M, Ishioka J, Saito K, Fujii Y. Who gains additional benefits from systematic biopsy concurrently performed with MRI-ultrasound fusion targeted biopsy in the detection of significant prostate cancer? The 34th Annual Congress of the European Association of Urology. Barcelona, Spain, 2019/3/16
Matsuoka Y, Uehara S, Yoshida S, Tanaka H, Fukuda S, Fukushima H, Moriyama S, Tanaka H, Kijima T, Yokoyama M, Ishioka J, Saito K, Fujii Y. Value of extra-target sampling for the detection of prostate cancer upgrading according to PIRADS scores. The 12th international symposium on focal therapy and imaging. Washington DC, USA, 2020/2/9
Uehara S, Matsuoka Y, Tanaka H, Tanaka H, Kijima T, Yoshida S, Yokoyama M, Ishioka J, Saito K, Fujii Y. Systematic biopsy cores near targets are of value for the detection of significant cancer: Analysis of prostate biopsy mapping using multiplanar MRI reconstruction. The 12th international symposium on focal therapy and imaging. Washington DC, USA, 2020/2/9
Matsuoka Y, Uehara S, Yoshida S, Tanaka H, Fukuda S, Fukushima H, Moriyama S, Tanaka H, Kijima T, Yokoyama M, Ishioka J, Saito K, Fujii Y. Who needs extra-target sampling in addition to intra-target sampling for the detection of adverse prostate pathology?: Spatial analysis of biopsy-proven cancer sites. AUA 2020
Matsuoka Y, Ishioka J, Tanaka H, Fukuda S, Fukushima H, Moriyama S, Uehara S, Tanaka H, Kijima T, Yoshida S, Yokoyama M, Saito K, Fujii Y. Apparent diffusion coefficient ratio as a quantitative imaging marker: Utility in a nomogram for predicting biochemical recurrence after radical prostatectomy. AUA 2020
Uehara S, Matsuoka Y, Tanaka H, Moriyama S, Tanaka H, Kijima T, Yoshida S, Yokoyama M, Ishioka J, Saito K, Fujii Y. Systematic biopsy cores away from targets are of limited value for the detection of significant cancer: Analysis of 3D prostate biopsy mapping using multiplanar MRI reconstruction. AUA 2020
Matsuoka Y, Uehara S, Yoshida S, Tanaka H, Tanaka H, Kijima T, Yokoyama M, Ishioka J, Saito K, Fujii Y. Value of extra-target prostate biopsy for the detection of MRI-missed adverse pathology according to PIRADS scores: spatial analysis of biopsy-core mapping using MR-ultrasound fusion images. in submission
Matsuoka Y, Uehara S, Yoshida S, Tanaka H, Fukuda S, Fukushima H, Moriyama S, Tanaka H, Kijima T, Yokoyama M, Ishioka J, Saito K, Fujii Y. Who benefits from extra-target sampling in addition to intra-target sampling for the detection of adverse prostate pathology?: Stereological analysis of biopsy-proven cancer sites. EAU 2020
Uehara S, Matsuoka Y, Tanaka H, Moriyama S, Tanaka H, Kijima T, Yoshida S, Yokoyama M, Ishioka J, Saito K, Fujii Y. Systematic biopsy cores away from targets are of limited value for the detection of significant cancer: Analysis of prostate biopsy mapping using multiplanar MRI reconstruction. EAU 2020

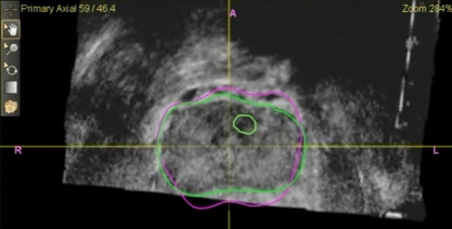
 弾性融合
弾性融合